Blandar

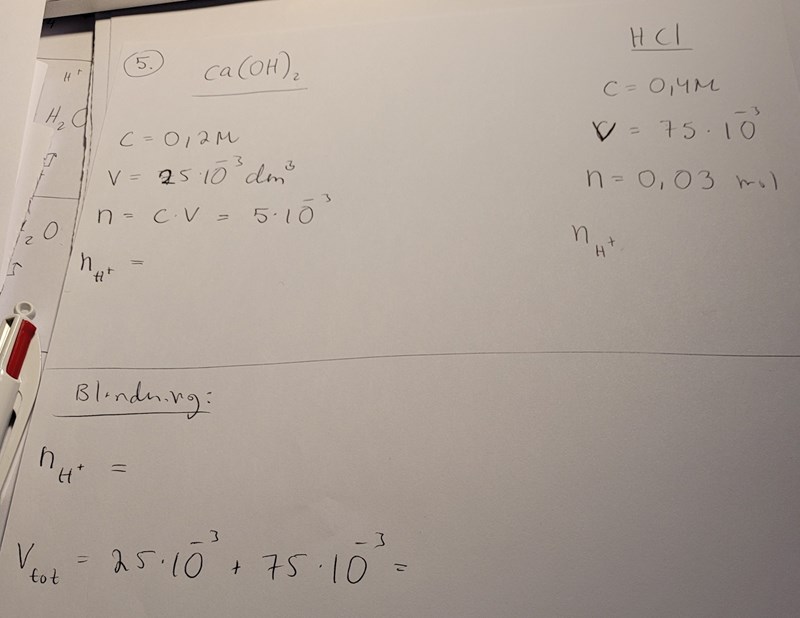 Jag behöver hjälp att lista ut substansmängden för väte för kalciumhydroxid och HCl.
Jag behöver hjälp att lista ut substansmängden för väte för kalciumhydroxid och HCl.
Hur många mol hydroxidjoner finns det i 1 mol kalciumhydoxid?
2?
Och blir förhållandet 1:1 för HCl, och om det är så varför?
Ja, det finns 2 mol hydroxidjoner i 1 mol kalciumhydroxid. Det betyder att du behöver räkna om hydroxidjonkoncentrationen för kalciumhydroxid innan du räknar om det till pH.
En HCl-molekyl har en vätejon som den kan avge (så att den tas upp av en vattenmolekyl, så att det bildas oxoniumjoner, som är det ämne som finns i alla sura vattenlösningar).
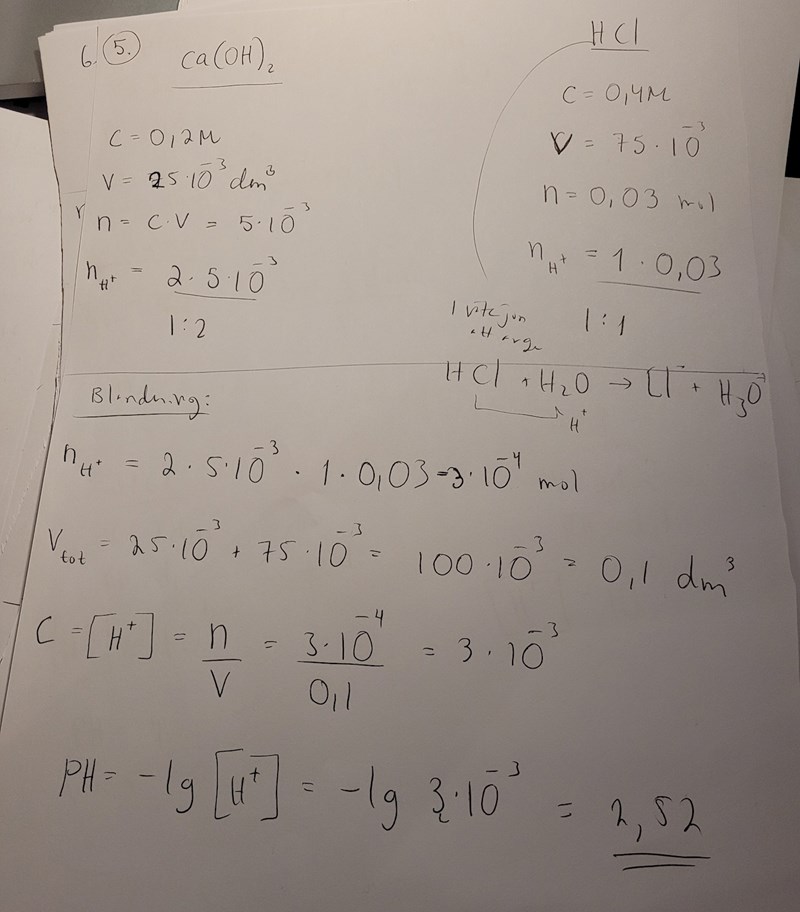 det ska bli pH= 0,70
det ska bli pH= 0,70
25 cm3 Ca(OH)2 med konc 0,20 mol/dm3 innehåller 0,025*0,20*2 = 0,010 mol hydroxidjoner
75 cm3 HCl med koncentrationen 0,40 mol/dm3 innehåller 0,075*0,40 = 0,030 mol oxoniumjoner
Om man blandar lösningarna får man 0,020 mol oxoniumjoner i en lösning med volymen 0,100 dm3.
Du verkar inte ha räknat ut substansmängden för hydroxidjoner, utan har räknat ut något annat och kallat det "substansmängden för vätejoner". Eftersom du inte har räknat ut hur mycket hydroxidjoner det fanns, har de inte kunnat reagera med oxoniumjonerna och neutraliserats.


