Energi
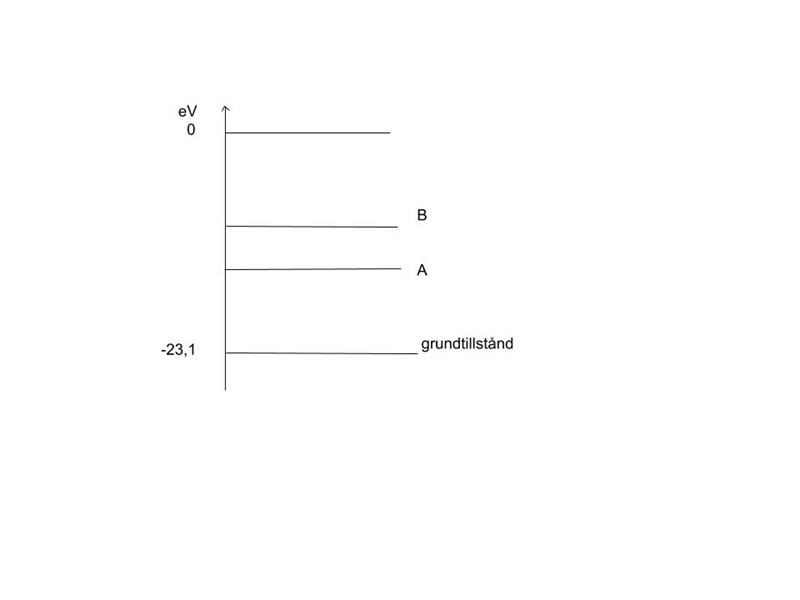
Figuren visar energinivådiagram för en tänkt atom. Då atomen övergår fre nivå A till grundtillstånd utsänds elektromagnetisk strålning av våglängden 190 nm. Då den övergår från nivå B till A utsänds strålning av våglängden 330 nm. Grundtillståndet har energin -23,1 eV
a.) Vilket våglängd har den strålning som emitteras då atomen övergår från nivå B till grundtillståndet?
b.)Vilka energier har nivåerna A och B?
kan någon hjälpa mig med denna uppgift? Jag tänkte att lösa första frågan genom att räkna energi i B och sen addera den med grundtillstånd men det stämmer inte riktigt med facit!
och i andra frågan jag använder formeln : E= h*c/våglängden
Det är rätt att använda formeln du anger.
Du får energiskillnaden mellan nivå A och grundtillståndet när du använder formeln med 190 nm och energiskillnaden mellan B och A med formeln och 330 nm. Då kan du bestämma energiskillnaden mellan B och grundtillståndet och därmed räkna ut våglängden på motsvarande strålning.
När du räknat rätt ska du se att svaret följer Rydberg-Ritz kombinationsprincip:
Så här menar ni? Det känns att det blir lite krångligt med beräkningar, hur bör jag räkna skillnaden? Och på min metod har svaret på frågan 2 innan 3 är det ok? 

Nja, inte exakt 117 nm.
Du gjorde förmodligen alldeles för stora avrundningar: https://www.google.com/search?q=1%2F%281%2F330+%2B+1%2F190%29+%3D
Jag förstår inte varför blir det 1/190+1/330 medan jag har följet formeln, kan du vissa gärna hur har du kommit fram till detta och vad är felet på mina beräkningar ?
Energiskillnaden är hc/lambda, som du använde.
Summan av två steg är efterfrågad. Dela med hc så får du formeln som Janne Rydberg och Ritz upptäckte.
Mycket mindre räknande, färre avrundningar på vägen.
Jag blir förvirrad egentligen, först sa du energi skillnaden sedan sa du summan av två steg. Kan du gärna visa hur du menar?
och jag tror att vi inte har formeln som Janne Rydberg och Ritz upptäckte i min fysik bok, så jag vet inte faktiskt vad det är kan du visa?
Vad är problemet?

Varför gjorde du inte en sådan ritning själv?
Din metod är ju lättare men jag vet inte hur ska jag använda det med andra uppgifter. Och det känns att jag har lite problem med beräkningar när jag vill beräkna energi skillnaden, vissa lärare subtrahera det minsta talet från det största och viss adderar det minsta med det största som jag har gjort. Då förstår jag inte vilken energi som är före och efter enligt lagen. Kan du gärna förklara till mig principen i beräkningar! Eller vissa vad har jag gjort fel för att kunna förstå bättre
Jag ber om ursäkt att jag frågar mycket men det är egentligen jättekrånglit.
Det är bara energiskillnader som är viktiga. Sådana uppgifter blir alltid lättare om man ritar.
Man kan också rita om energiskalan, lägga grundtillståndet på noll:
Jag tror att jag har förstått nu och kommit till rätt svar hoppas jag, tack för hjälpen!
Hur gör man uppgift b då?
Är det bara att räkna ut E för varje våglängd med formeln E=hc/lambda?
Då jag gör detta får jag inte samma energinivåer som är utmarkerade i bilden ovan
Jonne skrev:Då jag gör detta får jag inte samma energinivåer som är utmarkerade i bilden ovan
Då har väl jag eller du räknat fel. Jag har visat mina siffror, vad mer kan jag säga?
Pieter Kuiper skrev:Jonne skrev:Då jag gör detta får jag inte samma energinivåer som är utmarkerade i bilden ovan
Då har väl jag eller du räknat fel. Jag har visat mina siffror, vad mer kan jag säga?
Ja räknade fel kom på det nu


