Esterbildning
Varför är H2SO4 en katalysator för esterbildning mellan en alkohol och karboxylsyra?
I det första steget under den katalyserade esterbildningen så norpar ett fritt elektronpar på karbonylsyret i karboxylgruppen en proton. Denna ger karboxylgruppen större karbokatjonkaraktär och gör karbonylkolet mer elektrofilt. Detta påskyndar attacken från alkoholens OH-grupp:
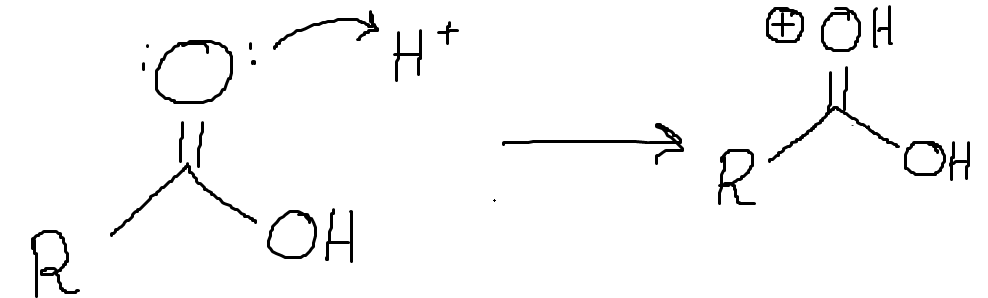
När syret får en formell laddning +1 kommer den börja dra hårdare i kolets elektroner, och då blir denna givetvis mer elektrofil. Detta möjliggör en nukleofil attack från alkoholen.
Bara för att förtydliga mitt tidigare inlägg, om det inte var tydligt: detta sker inte under en icke-katalyserad estersyntes. Under en icke-katalyserad estersyntes så attackarerar alkoholen karbonylkolet ändå, men detta sker långsammare eftersom karbonylkolet har mycket mindre karbokatjonkaraktär.
Tack!



