Formel balansering
Jag har en till:
''Skriv formel för upplösning a magnesium i utspädd salpetersyra. Här reduceras nitratjonerna till dikväveoxid.''
Jag skrev:
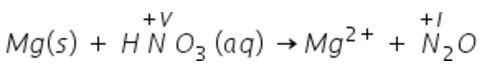
Magnesium oxideras i två steg och avge 2 elektroner:
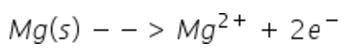
Kväve reduceras i 4 steg:
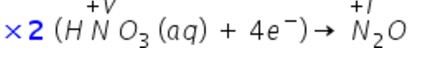
Så allt som innehåller magnesium har jag mutiplicerat med 4.
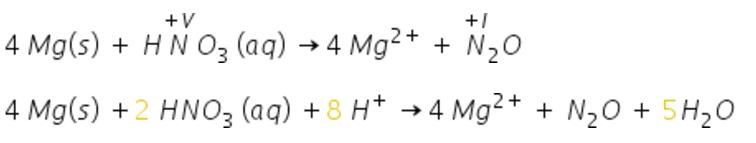
Laddningarna är + 8 på Vl och + 8 på HL, så den borde stämma?
Bocken säger nåt helt annat!
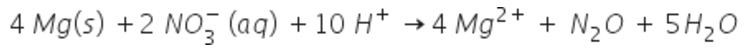
och lägger till en komplettering med

Du har samma lösning som boken.
Jämfört med bokens lösning har du tagit två av vätejonerna och slagit ihop dem med de två nitratjonerna till salpetersyra.
Logiskt är uttrycken ekvivalenta, men frågan är om kemister föredrar bokens svar. Bokens slutgiltiga svar utan en massa laddningar utskrivna känns kanske "snyggast".
Jag tycker att det är ganska komplicerat ändå.. Su menar att det kastades åskådare joner för att undvika magnesium joner?
existerar inte, eftersom salpetersyra är en stark syra (d v s så fort en salpetersyramolekyl kommer i kontakt med en vattenmolekyl så reagerar de med varandra och bildar en nitratjon och en oxoniumjon). Väldigt konstigt om de skriver så i boken. Möjligen vill de mena det ungefär som man skriver NaCl(aq) trots att man vet att natriumkloriden är uppdelad i sina joner.
Ok...Vad är en oxonjon?
Oxoniumjon . Ibland pratar men om vätejoner men det är inte riktigt sant i vattenlösning, för vätejonern reagerar omedelbart med en vattenmolekyl så att det bildas en oxoniumjon. När man skriver i reaktionsformler gör man det för att det skall synas tydligare, utan en massa vattenmolekyler som skymmer.
Ah just det, det råkade jag också glömma. Tack Smaragdalena!




