Fråga om tolkning av punkter i VLE-diagram
Hej!
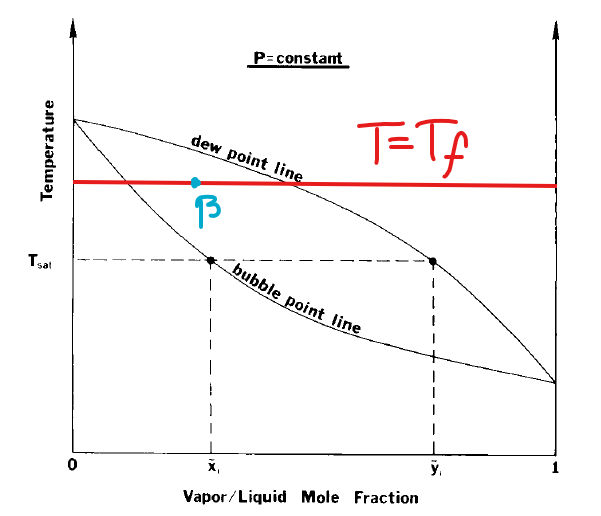
Låt oss säga att vi studerar ett VLE-diagram:

Något jag inte riktigt begriper är vilka punkter som faktiskt ingår i detta diagram och inte. Ingår punkterna som ligger innanför arean som avgränsas av bubbelpunktslinjen och daggpunktslinjen? Ingår alla punkter utanför? Jag vet att under bubbelpunktslinjen är blandningen i vätskefas och ovanför daggpunktslinjen är blandningen i gasfas. Då verkar det som om alla punkter ingår. Men vad händer innanför linjerna?
Punkterna får du längs med linjerna (line i figuren). Det är väl mest ett sätt att sätta de två linjerna i ett och samma diagram, för avläsning/sambandsorsaker. Kopplingen mellan diskreta punkter fås direkt (som i bilden där temp vs molfraktionerna ses). Ändrar du temperaturen ändras bägge molfraktionerna. Arean mellan linjerna skulle jag säga är utan funktion, utan uppstår endast i.o.m. att det är två linjer som plottats tillsammans.
Hmm, okej. Anledningen till att jag frågar är följande: låt säga att vi börjar med en blandning helt i vätskefas med molbråk av komponent 1 som i bilden. Vi höjer sedan temperaturen successivt utan att nå bubbelpunktslinjen. I och med att vi höjer temperaturen, och alltså ”rör oss vertikalt uppåt” ligger vi alltid på en tillåten punkt i diagrammet då?
Sedan låter vi temperaturen stiga ytterligare till bubbelpunktslinjen. Kommer molfraktionen i vätskefas då ändras, dvs. vi kan inte bara fortsätta röra oss upp i diagrammet utan vi måste röra oss längs linjen med stigande temperatur?
Fick ta en titt och fundera lite till. Under den bubblepunktslinjen har vi vätska, och ovanför daggpunktslinjen finns endast ånga. Arean mellan linjerna är den fasen då det finns en vätska/ångjämnvikt, "VLE". Linjerna är väl även mättnadsgränsen för vätskan (bubbelpunktsl.) och gasen (daggpunktsl.).
Vid ditt exempel där vi utgår ifrån en punkt under bubbelpunktslinjen, så "rör vi oss vertikalt uppåt" tills att bubbelpunktslinjen nås och ånga av ämnet (A) bildas, och det finns en hög andel av (A) i både ångan och de bildade kondensdropparna. Ökas temperaturen ytterligare kommer sammansättningen av både vatten och gasfasen ändras. Mer av (A) som dunstar till gasfasen, och samtidigt kommer molbråket minska för båda faserna, vid en tänkt horizontell linje lite högre upp. Och detta fortsätter tills vi går utanför daggpunktslinjen då allt istället finns i gasfasen.
Så om vi har en temperatur som som är sådan att linjen har punkter som ligger ”mellan bubbelpunkts- och daggpunktslinjerna”, är de punkterna tillåtna eller ingår de inte? Jag kan inte rita en graf nu men jag hoppas min fråga framgår.
EDIT: nu kan jag rita. Är t.ex. den blå punkten en möjlig punkt i grafen eller är det bara punkterna på den röda linjen som korsar bubbelpunkts- och daggpunktslinjen som är möjliga punkter givet temperaturen?
En till fråga jag har om detta: är det verkligen rätt att kalla temperaturerna som bubbelpunkts- och daggpunktslinjen ligger på för "kokpunkter"? Jag har sett det flera gånger men det verkar vara grovt missbruk av terminologi. Det finns ju många temperaturer som ligger under en vätskas "kokpunkt" där det ändå existerar en ångfas och en vätskefas i jämvikt...
naytte skrev:Så om vi har en temperatur som som är sådan att linjen har punkter som ligger ”mellan bubbelpunkts- och daggpunktslinjerna”, är de punkterna tillåtna eller ingår de inte? Jag kan inte rita en graf nu men jag hoppas min fråga framgår.
EDIT: nu kan jag rita. Är t.ex. den blå punkten en möjlig punkt i grafen eller är det bara punkterna på den röda linjen som korsar bubbelpunkts- och daggpunktslinjen som är möjliga punkter givet temperaturen?
Punkten beta är möjlig vid den temperaturen. Det är då en blandning mellan gasformigt ämne och vätskeformigt ämne fas i gasfasen, vid den temperaturen och molbråket. Det gäller även för resten av molbråken mellan α och γ (längs gröna linjen), men sammansättningen i gasen/dropparna i gasen skiljer längs gröna linjen.

Molbråket för beta är olik från bubbelpunktslinjen respektive daggpunktslinjen vid den temperaturen. Vid denna temperatur kommer ångan som bildas ha sitt eget molbråk (α) och samma sak med molbråket för den vätska som kondenserar (γ). I princip finns det ånga/droppar i gasfas längs den gröna linjen, men innanför bubbel-/daggpunktslinjerna (längs gröna linjen).
Diagrammet visar situationen vid ett slutet system, och VLE används vid destillationer där syftet är att minska öka koncentrationen (molbråket) av ämnet. T.ex. vid Tsat kommer molfraktionen som lämnar vätskan vara ~0,25 medans molfraktionen i kondensatet kommer vara ~0,75. Samlas kondensatet upp separat (t.ex. genom avledning till ett externt kärl) kommer ämnet att anrikas i destillatet, och minska i vätskan, d.v.s. ett mer koncentrerat destillat fås och ursprungsvätskans koncentration av ämnet minskar. Och när molbråket i vätskan ändras (genom att ämnet lämnar systemet) kommer allt flyttas successivt åt vänster fram tills bubbelpunktslinjen nås.
Edit: infogade bilden jag glömde, samt korrigerade.
naytte skrev:En till fråga jag har om detta: är det verkligen rätt att kalla temperaturerna som bubbelpunkts- och daggpunktslinjen ligger på för "kokpunkter"? Jag har sett det flera gånger men det verkar vara grovt missbruk av terminologi. Det finns ju många temperaturer som ligger under en vätskas "kokpunkt" där det ändå existerar en ångfas och en vätskefas i jämvikt...
Jo men när ämnet lämnar vätskefasen sker det som ånga och man kan väl tänka sig att det även bildas aerosoler, och ämnet kan sedan finnas kvar som ånga som står i jämvikt med droppar i gasfasen. Så tekniskt sett är det väl okej med säga att det är kokpunkter längs bubbelpunktslinjen. Längs daggpunktslinjen kondenserar ämnet från gasfasen till vätska igen, men denna mängd ämne står ju i jämvikt med gasfasen, så att det "kokar" från kondensationsytan tillbaka till gasen går väl att beskriva med kokpunkt? Har inte riktigt funderat på detta, men det låter inte helt knasigt för min del i alla fall.


