Hur skulle man principiellt lösa samma problem i Helmholtzformalismen?
Hej!
Låt oss anta att vi studerar ett enkelt termodynamiskt system (eng: simple system) med ett kemiskt species som består av två delsystem där delsystemen initialt är separerade av en adiabatisk, icke-permeabel och orörlig vägg:
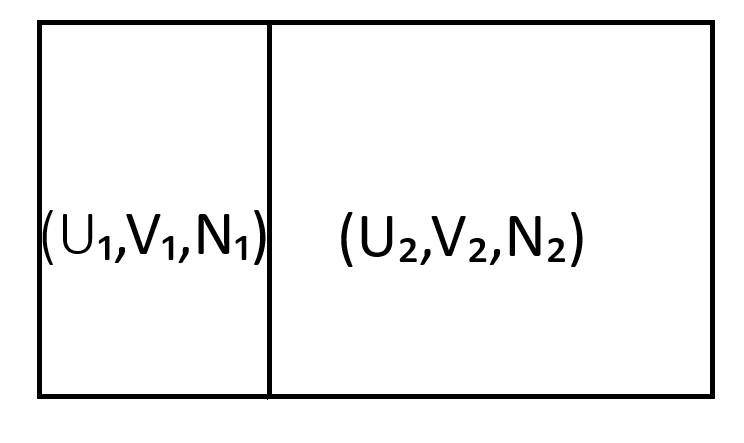
Det som jag nu huvudsakligen vill diskutera i denna tråd är den bredaste varianten av det som ibland kallas för "the basic problem of thermodynamics": om vi häver alla interna begränsningar, alltså gör väggen som separerar delsystemen diaterm, permeabel och rörlig, hur ser då den nya fördelningen av energi, volym och moltal ut vid jämvikt?
För att besvara denna fråga kan vi åberopa entropimaximeringsprincipen, som följer nedan:
Entropimaximeringsprincipen. Entropin för ett system har egenskapen att systemets interna parametrar antar de värden som maximerar entropin över mångfalden av begränsade jämviktstillstånd och som är konsistenta med de befintliga begränsningarna.
Om vi tillämpar denna princip får vi ett system av ekvationer vars lösningar ger oss svar på vår fråga. Entropin är additiv över de två delsystemen och kan skrivas som med , och .
Om vi bildar differentialen och undersöker extremumvillkoret :
Med typiska beteckningar får vi alltså , och , och lösning av dessa ekvationer ger oss våra jämviktsfördelningar.
För ett system kan vi allmänt lösa ut ur den den fundamentala relationen och erhålla . Om vi Legendretransformerar denna funktion med avseende på entropin erhåller vi en funktion som innehåller samma information om systemet men tar entropins konjugatvariabel — temperatur — som oberoende variabel. Vi kallar denna funktion för Helmholtz fria energi .
Man kan med ganska enkla argument visa följande sats:
Helmholtzminimeringsprincipen. Helmholtz fria energi för ett system har egenskapen att om systemet är i kontakt med en temperaturreservoir, så antar systemets interna parametrar de värden som minimerar över mångfalden av begränsade jämviktstillstånd och som är konsistenta med de befintliga begränsningarna.
Låt oss anta att sätter vårt system i kontakt med en temperaturreserovir. Tillämpning av denna princip ger precis som tidigare, med lite trixande (vi måste lista ut hur vi ska tolka derivatorna som dyker upp då vi bildar differentialen ), och . Tillsammans med bivillkoren och kan vi i princip lösa ut i jämvikt, alltså två av de tre storheterna vi behöver för att karaktärisera jämviktstillståndet för delsystemen. Det saknas alltså en storhet, nämligen energin.
Hur ska vi göra om vi också vill veta och ? Helmholtz fria energi innehåller ju exakt samma termodynamiska information som entropin, så det känns ju som om man borde kunna lösa ut dessa storheter genom tillämpning av Helmholtzminimeringsprincipen som ovan, men jag förstår inte riktigt hur.
Har någon några bra idéer här? Samma fråga har jag för övrigt för alla andra termodynamiska potentialer, där man Legendretransformerar fler variabler.


