Joner i tetraedriska och oktaedriska hål

I problemtexten står det fel längd. Längden ska vara 1420 pm.
Jag har räknat ut radien på Buckminsterfulleren genom pythagoras sats:
På b-uppgiften förstår jag inte så mycket dock. Radien för K+ är enligt tabellvärde 138 pm, men vet inte hur jag ska gå vidare för att ta reda på vilken typ av hål som innehåller K+ och hur stor andel av hålen som är fyllda...
Radien verkar ju ha blivit korrekt. I b) måste du beräkna radiekvoten som i detta fall blir 138/502=0,2749… och jämföra det med minsta radiekvot för de olika strukturhålen. Enligt min formelsamling så innebär det att kaliumjonerna helst lägger sig i tetraediska hål. I så fall innebär det att de oktaedriska hålen är för stora (eller omvänt - att kaliumjonerna är för små) och att det då blir större repulsion mellan anjonerna.
Det finns fyra anjoner, fyra oktaedriska och åtta tetraediska hål per enhetscell. Eftersom man enligt stökiometrin behöver 4*3=12 kaliumjoner för att få en neutral förening behöver man fylla alla tetraediska och sen även alla oktaedriska hål för att få till en neutral förening. Så svaret bör vara att alla tetraediska och oktaedriska hål är fyllda.
Teraeagle skrev:I b) måste du beräkna radiekvoten som i detta fall blir 138/502=0,2749… och jämföra det med minsta radiekvot för de olika strukturhålen. Enligt min formelsamling så innebär det att kaliumjonerna helst lägger sig i tetraediska hål. I så fall innebär det att de oktaedriska hålen är för stora (eller omvänt - att kaliumjonerna är för små) och att det då blir större repulsion mellan anjonerna.
Finns det alltså färdiga värden på minsta radiekvot för olika strukturhål?
Och hur vet man att de tetraedriska hålen är mindre? Är det för att de inte sammanfaller med ett hål i "nästa lager"?
Ja det finns tumregler för det som du borde ha någonstans i ditt kursmaterial.
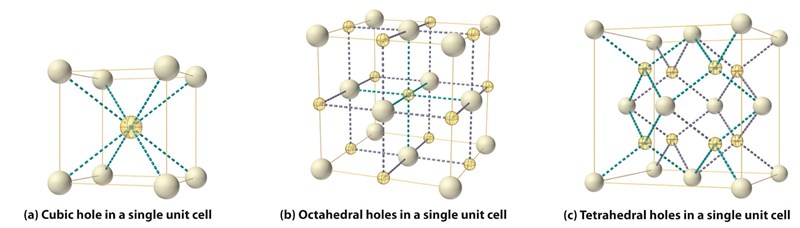
Ett oktaedriskt hål omges av sex atomer medan ett tetraediskt hål omges av fyra atomer enligt bilden ovan, så man kan få plats med fler tetraediska hål per enhetscell vilket också innebär att de måste vara mindre än oktaedriska hål.
Teraeagle skrev:Ja det finns tumregler för det som du borde ha någonstans i ditt kursmaterial.
Har det något att göra med strukturen på kristallen? Jag har radiekvoter för när det bildas NaCl-struktur/CsCl-struktur/SZn-struktur, men kan inte riktigt koppla det till tetraedriska respektive oktaedriska hål på rak arm.
Uppdatering: Jag tror jag fattar! Det måste ju vara tetraedriska hål i CsCl-struktur i och med att det är bcc och oktaedriska hål i NaCl-struktur i och med att det är fcc. Tänker jag rätt eller missar jag något?
Precis, det är bara andra namn för samma sak.
CsCl-struktur innebär att man har kloridjoner med cesiumjoner i de kubiska hålen
NaCl-struktur innebär att man har tätpackade kloridjoner med natriumjoner i de oktaedriska hålen
ZnS-struktur innebär att man har tätpackade sulfidjoner med zinkjoner i de tetraediska hålen
Då har jag bara ett sista frågetecken. Hur visste du att det är 4 oktaedriska hål och 8 tetraedriska hål per enhetscell i uppgiften? Jag tänker att det måste bli SZn-struktur då radiekvoten < 0,4, men tycker att det är svårt att tänka mig hur det ser ut och vilka hål som eventuellt finns.
Ett oktaedriskt hål har ett koordinationstal på 6, vilket innebär att det omges av sex sfärer (joner/atomer). Om du kollar på min bild i inlägg #4 så ser du det i b-figuren. Det enklaste är att titta på den jon som ligger i hålet i mitten, där kan man tydligt se att den omges av sex andra joner. Sen måste man även inse att man har "delar av hål" på kanterna av enhetscellen. Det finns ett helt hål i mitten, 1/4 hål på alla tolv kanter (dvs 12*1/4=3 hål). Totalt finns alltså 4 oktaedriska hål per enhetscell.
Tack så mycket för hjälpen!! Betydligt bättre förklarat än övningsledarna :)



