Kemi 1

Hade jag kunnat få hjälp med 7.16? Jag har redan gjort en del, dock vet jag inte hur jag ska fortsätta.
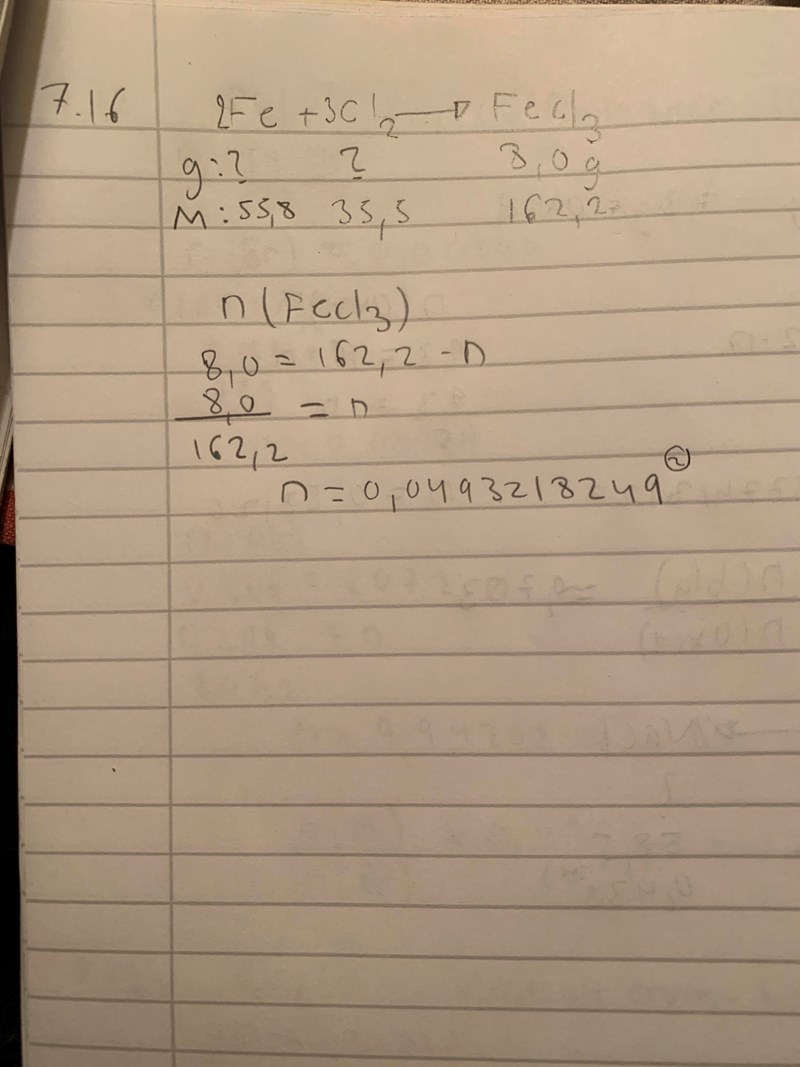
Formeln är inte balanserad på reaktantsidan. Dina beräkningar hittills ser rimliga ut. Vilket är molförhållandet mellan kloret och järnkloriden?
Edit: Produktsidan, jag är trött idag.
Smutstvätt skrev:Formeln är inte balanserad på reaktantsidan. Dina beräkningar hittills ser rimliga ut. Vilket är molförhållandet mellan kloret och järnkloriden?
Är du säker att formeln ej är balanserad? För i facit står det denna formel. Molförhållandet mellan klotet och järnkloriden vet jag ej. Hur räknar jag ut den?
Smutstvätt skrev:Formeln är inte balanserad på reaktantsidan. Dina beräkningar hittills ser rimliga ut. Vilket är molförhållandet mellan kloret och järnkloriden?
Oj såg vad som ej var balanserat nu. Tack så mycket!
Student02 skrev:Smutstvätt skrev:Formeln är inte balanserad på reaktantsidan. Dina beräkningar hittills ser rimliga ut. Vilket är molförhållandet mellan kloret och järnkloriden?
Är du säker att formeln ej är balanserad? För i facit står det denna formel. Molförhållandet mellan klotet och järnkloriden vet jag ej. Hur räknar jag ut den?
Produktsidan ska det vara. Jag är lite trött idag. :) Förhållandet kan du beräkna genom reaktionsformeln. Hur många mol klor krävs för att bilda en mol järnklorid?
Smutstvätt skrev:Student02 skrev:Smutstvätt skrev:Formeln är inte balanserad på reaktantsidan. Dina beräkningar hittills ser rimliga ut. Vilket är molförhållandet mellan kloret och järnkloriden?
Är du säker att formeln ej är balanserad? För i facit står det denna formel. Molförhållandet mellan klotet och järnkloriden vet jag ej. Hur räknar jag ut den?
Produktsidan ska det vara. Jag är lite trött idag. :) Förhållandet kan du beräkna genom reaktionsformeln. Hur många mol klor krävs för att bilda en mol järnklorid?
I facit står det : 3/2 * 0,0493
förstår ej hur de Fick fram 3/2? De delade n(Cl2)/n(FeCl3)
Ja, de beräknar molförhållandet , vilket alltså blir 3/2, då det krävs tre mol klor för att bilda två mol järnklorid.
Smutstvätt skrev:Ja, de beräknar molförhållandet , vilket alltså blir 3/2, då det krävs tre mol klor för att bilda två mol järnklorid.
Men hur blir det 3/2? Hur räknar de fram det? Är så förvirrad :(
De utgår från reaktionsformeln. Tre mol klor krävs för att bilda två mol järnklorid. Det ger molförhållandet 3/2.
Smutstvätt skrev:De utgår från reaktionsformeln. Tre mol klor krävs för att bilda två mol järnklorid. Det ger molförhållandet 3/2.
Tack så himla mycket för all hjälp! Men hur vet man det? Är det bara för att det är 3Cl2 och 2FeCl3?
Varsågod! Ja, precis. Molförhållandena går att utläsa från alla balanserade reaktionsformler. :)


