Kemiska beräkningar
 Hej behöver hjälp med denna uppgiften!
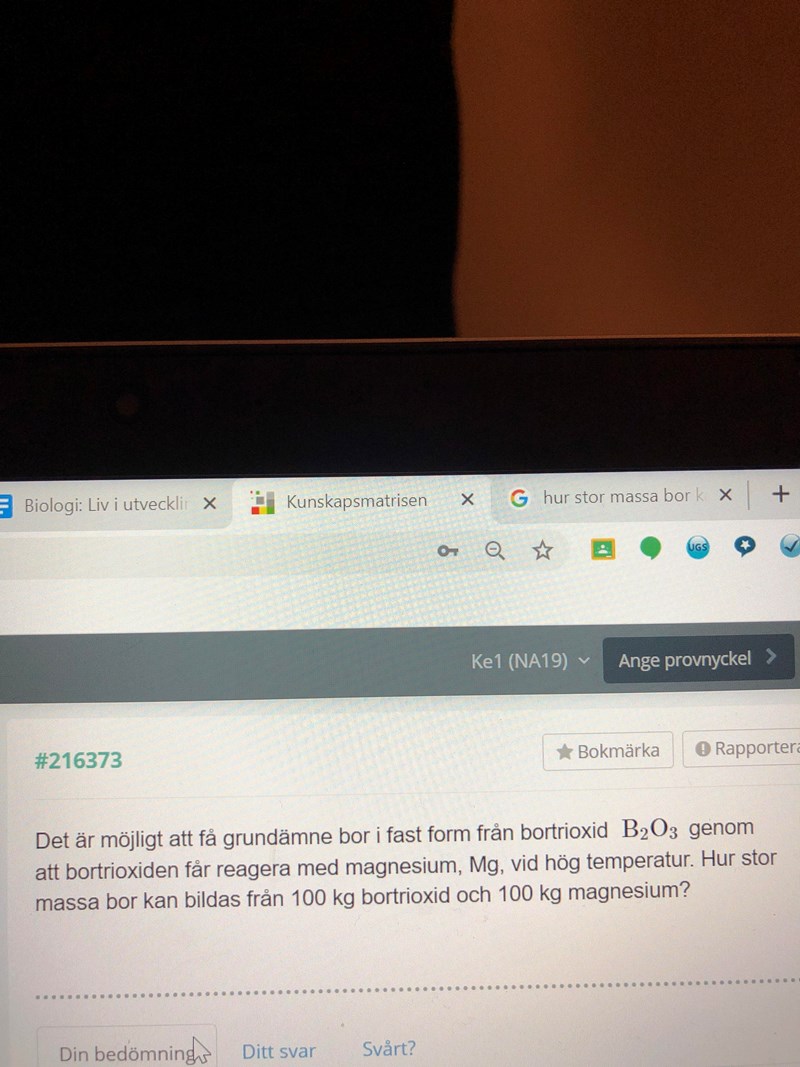
Hej behöver hjälp med denna uppgiften!
Jag började med att räkna substansmängden för mg (~4114mol) och B2O3 (~1700mol)
men kan ej fortsätta
Börja alltid med med en balanserad reaktionsformel för en överblick.
I detta fall blir det B203 + 3 Mg ---> 3 MgO + 2B
Här ser du att för varje mol B2O3 krävs 3 mol Mg i reaktionen. Detta innebär att en av reaktanterna rimligtvis tar slut först, i detta fall tar magnesiumet slut. Hur mycket B2O3 kan reagera med den mängden Mg som finns om förhållandet är 1:3?
Om du löser detta så kan du även räkna ut hur mycket B som bildas och slutligen vikten
Det känner jag till, för varje mol B2O3 behövs tre gånger mer Bor. Kan fortfarande inte gå vidare :((
Soso skrev:Det känner jag till, för varje mol B2O3 behövs tre gånger mer Bor. Kan fortfarande inte gå vidare :((
Nej, för varje mol B2O3 krävs 3 mol Mg. Detta innebär att 4114 mol Mg räcker för att reagera med ungefär 1370 mol B203 (4414/3). Hur mycket B bildas av 1370 mol B2O3 om molförhållandet är 1:2? Vad väger denna mängd B?
är det rätta svaret 29629,584g? Isåfall har jag beräknat rätt och kan förklara hur jag tänkt.
solskenet skrev:är det rätta svaret 29629,584g? Isåfall har jag beräknat rätt och kan förklara hur jag tänkt.
Utan att räkna på det kan jag säga att det inte är rätt svar - det är alldeles på tok för många siffror. Med en så välvillig tolkning som möjligt är det tre värdesiffror, vill man vara på den säkra sidan är det bara en.
jag skulle kunna avrunda svaret till 29630g.
solskenet skrev:jag skulle kunna avrunda svaret till 29630g.
Det är fortfarande för många värdesiffror, och en olämplig massenhet.
Vill gärna veta vart felet är i min uträkning
Du använder fel molmassa för magnesium.
oj molmassan är 24,305g/mol. Är tankesättet annars rätt? bortsett från att jag råkat använda mig av fel molmassa?
Bortsett från att du har för många värdesiffror i svaret och fel molmassa så ser det rätt ut. Bra och tydlig redovisning där du beskriver vad du gör.
Om du hade fått fram 17 867 gram med rätt uträkning hade det varit lämpligare att svara 18 kg.



