Oxidationsreaktion- vilket ämne avger vad?
I följande reaktion så oxideras etanol och syrgas reduceras och bildas etanal och vatten.
2C2H5OH + O2 --> 2CH3CHO + 2H2O
I beskrivningen till följande reaktion står det att etanolmolekylen oxideras genom att den avger totalt 4 väteatomer (med tillhörande elektroner) till syret. Är oxidationen att 4 väteatomer avges? För att de innehåller elektroner? I så fall är ju typ alla reaktioner oxidationer? Fortsätter man läsa beskrivningen så står det att det egentligen är det kolet som är bundet till syret som oxideras och att man skulle se detta om man skrev ut oxidationstal. Vad innebär det? Att det är elektroner bundna till kolet som avges? Hur kan den göra det? Kolet har ju 4 valenselektroner och alla är upptagna i bindningar, om den avger någon elektron så bryts väl bindningarna? Jag är inte så duktig på oxidationstal men jag hittade denna bilden på nätet:
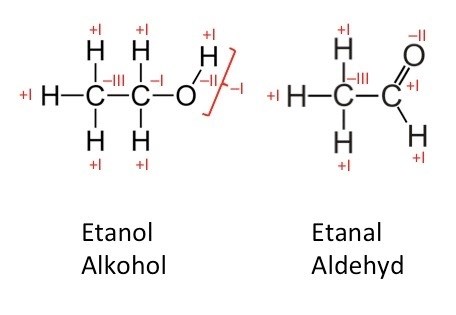
Och där ser jag ju att oxidationstalet har ökat från -1 till +1, alltså att den ska ha avgett 2 elektroner och sedan är det multiplicerat med 2 antar jag eftersom att det är 2 molekyler i min ekvation, så det blir 4 elektroner totalt. Jag förstår dock inte hur det "fungerar i praktiken" eller vad man ska säga. Stämmer det att kolet avger 4 elektroner? Hur kan den isåfall göra det? Och är det då det som är själva oxidationen egentligen, inte att det är väteatomer som innehåller elektroner som avgetts?
Känns som att det var många funderingar där… Men generellt så betyder oxidation att ett ämne förlorar elektroner. Det kan ske fullständigt, t.ex. när klorgas oxiderar natrium så att det bildas kloridjoner och natriumjoner. Det kan också ske partiellt, som i detta fall. Då menas att någon atom i ämnet har ökat sitt oxidationstal vilket innebär att den har ”delvis förlorat” elektroner. Inte tillräckligt för att bindningarna ska brytas, men elektronerna har förskjutits mot någon annan atom.
Om man kollar på kolatomen som oxideras i ditt exempel så binder den först med en av sina elektroner till syre, en till ett annat kol och två till väte. I kol-kol-bindningen ligger bindningselektronerna mitt emellan kolatomerna. I väte-kol-bindningarna ligger elektronerna lite närmare kolatomen eftersom kol är mer elektronegativt än väte. I syre-kol-bindningen ligger elektronerna mycket närmare syre eftersom syre är mycket mer elektronegativt än kol.
I fallet etanal har man istället två bindningselektroner från kolatomen som binder till syret (en dubbelbindning), en till väte och en till kol. Här har man alltså en situation där två av bindningselektronerna ligger långt från kolatomen i fråga, medan en ligger ganska nära medan den sista ligger mitt emellan. På det stora hela ligger alltså elektronerna i snitt längre bort från kolatomen i etanal än i etanol. Det är det man menar med att kolatomen, eller något oegentligt ”etanol” har oxiderats. Man kan se det som att den har förlorat inflytande över sina elektroner eftersom det har uppstått en extra bindning till elektronegativa syret.


