Sn1 laboration
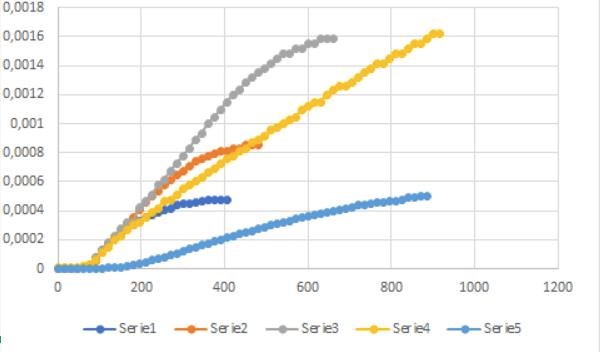
Detta är en laboration med tertiär butylklorid och teoretiskt sätt ska det vara reaktionstypen Sn1 för detta, det stämmer på alla förutom serie 4. I serie 4 så har man en etanol och vattenlösning (1:1). Det skedde något fel med tillsättning av tert-butylklorid men om man kollar på oxoniumjonkoncentrationen (som är på y sidan, x är tiden) så kan man utgå från att man måste ha tillsatt ungefär lika mycket som i serie 3. Frågan jag då har är hur kan det komma sig att reaktionshastigheten blev söligare på serie 4 än på serie 3, eftersom det är en Sn1 reaktion borde ju inte nukleofilens koncentration påverka reaktionshastigheten? Har någon stött på något liknande och kanske kan förklara eller ska man bara utgå från att flera felkällor orsakade detta? Temperaturen för båda reaktionerna var ungefär lika, kan ha varit 2 grader skillnad men isåfall var det högre på serie 4 och då borde reaktionen ha gått snabbare.
Tack på förhand)))
Uppriktigt sagt är det svårt att få ett grepp om vad dina data motsvarar, och vad du faktiskt har gjort.
Vi kan inte se vilken reaktion detta är (formel saknas, reaktionsförhållandet för de flesta serier är inte angivet)?
Hur du följer reaktionen?
Vilken skillnad det är mellan de fyra serierna som du har ritat ut för att jämföra?
Vilket resultat hade du väntat dig?
Vad avviker ifrån ditt väntade resultat, varför misstänker du att det avviker? Kan du gissa varför det avviker?
Så om du ger mer information, kanske vi kan ge mer återkoppling och hjälpa dig vidare.
Reaktionen som skedde var en substitutionsreaktion med tertiär butylklorid (som substrat) och vatten (som nukleofil). I serie 1 har man 100 cm3 vatten och 5 droppar substrat, i serie 2 100 cm3 vatten och 10 droppar substrat och i serie 3 100 cm3 vatten och 15 droppar substrat. Sedan i serie fyra har man 50cm3 etanol och 50 cm3 vatten och det ska vara 5 droppar substrat (men här blev det en felkälla och det måste ha kommit in mer substrat, typ 15 droppar eftersom koncentrationen på oxoniumjonerna blev som på serie 3). Om man då utgår från att det är 15 droppar substrat i serie 4 så är väl det förväntade resultatet att det ska bli en likadan graf som på serie 3 eftersom nukleofilens koncentration (vattnets koncentration) inte ska spela någon roll. Detta är vad som avviker, reaktionshastigheten för serie 4 är söligare, men borde inte vara det eftersom det är en SN1 reaktion som ska ske eftersom vi laborerade med en tertiär haloalkan.
Det är ju bara i SN2 reaktioner som nukleofilen ska påverka reaktionshastigheten. Och reaktionshastigheten på graferna är deras lutning, ju mer lutning desto snabbare sker reaktionen. Det enda jag kunde förklara är varför det blev högre oxoniumjonkoncentration är förväntat (just för att det fanns mer substrat än man egentligen skulle ha), men varför reaktionshastigheten blev annorlunda vet jag inte. Kan de ha något med etanolens påverkan på vattnets egenskaper eller?
Hoppas det var lite lättare att förstå))
Oavsett om det var 5 eller 15 droppar i serie 4, är det uppenbart att etanolen påverkar hastigheten.
Det går långsammare än serie 3 (15 droppar), men reaktionen pågår fortfarande efter 900 sekunder.
Det går lite långsammare än serie 1 (5 droppar), och reaktionen pågår längre (serie 1 planar ut redan efter 400 sekunder).
Resultattolkningen blir helt annorlunda on det är 5 droppar tertiär butylklorid, eller om det är 15 i serie fyra.
Är det faktiskt var 5 droppar, ser du att reaktionen pågår längre för serierna 3 och 4 - kurvan fortsätter öka över 0,001. Serierna 1 och 2 planar ut tidigare (och det är väl därför flera data punkter inte samlats efter 500 enheter på y-axeln). Det ser till och med ut som om reaktionen kan fortsätta ytterligare för serie 4 - den kurvans tangent har inte avvikit vid de sista datapunkterna - kurvan är fortfarande linjär och ökar.
Om du vet med dig att du/dina medlaboranter tillsatte 15 droppar får vi diskutera detta istället. Men du riskerar att lura dig själv i resultattolkningen om du istället "hittar (på) 15 droppar som felkälla" för att förklara resultatet.
Nej, kurvorna stannar av där jag stoppat dem eftersom pH värdet ej förändrats på ett tag, valde bara att inte skriva ut det. Och eftersom etanolen egentligen INTE ska påverka reaktionshastigheten var jag tvungen att hitta andra felkällor. Detta är en Sn1 reaktion och det ska därför ej påverkas av nukleofilen (vattnets förändring). Vi vet ej hur många droppar vi tillsatte för att vi inte hade automatpipett utan det kan ha kommit mer så därför måste feldroppning vara ett alternativ för felkälla.
Jag tror inte att vi kommer någon vart med detta för att det är svårt att förklara vad jag vill ha hjälp med så kan jag radera denna tråd (tror inte den kan vara till hjälp för någon)?
Mvh
Hej
Vad tråkigt att du inte kände att du lyckades nå fram dit du ville. Jag tycker inte du ska ge upp men oavsett så får tråden ligga kvar Vi har som policy att inte radera trådar som blivit besvarade, om det inte finns särskilda skäl för det.
/Jonto, moderator
Eftersom halva volymen är etanol i serie 4, påverkar alkoholen hur vattnet och tert-butylkloriden beter sig. Är det bara vattenmolekyler kommer de att vätebinda lite annorlunda, till skillnad från om de även vätebinder till etanol. Det var det jag försökte förmedla. Dock verkar det bildas minst lika mycket produkt för både C och D serierna, så det talar för att det finns liknande/samma mängd tert-butylklorid i båda proverna.
Samtidigt kan etanolen faktiskt agera som nukleofil den med (den har sin hydroxigrupp som kan bilda en bindning till karbokatjonen, men etanolen är en sämre nukleofil än vatten).
Men det ser ut att bildas lika mycket produkt i serierna 3 och 4.


