Termodynamik - vad är kokning?
Hej!
Jag har en fråga som känns uppenbar intuitivt men som jag inser att jag faktiskt inte förstår: vad innebär kokning?
Diverse källor på internet säger att kokning är det fenomen som uppstår då en vätskas ångtryck blir lika stort som omgivningens tryck. I fallet med vatten får vi alltså kokning vid ca. vid vanligt atmosfärstryck. Men jag har lite svårt att förstå det här med ångtryck.
I en icke-permeabel behållare definieras ångtrycket i den litteratur jag har läst som ångfasens tryck vid den temperatur där ångfasen står i termodynamisk jämvikt med vätskefasen. Detta tryck är lika stort som vätskefasens tryck. För ett rent ämne är en sådan fasjämvikt endast är möjlig vid en temperatur, och således borde det bara finnas ett "ångtryck" att tala om. För en vätskeblandning med flera komponenter finns det ett intervall av sådana temperaturer.
De temperaturer där en sådan jämvikt är möjlig kallas ofta för "kokpunkter". Så jag har två frågor:
- Vad är kokning? Är det helt enkelt fasövergången från vätskefasen till ångfasen? Innebär det i så fall att vatten förorenat med luft kan "koka" vid (eftersom det bildas ånga)?
- Vad skulle ångtryck vara utan kokning? Så som begreppet är definierat finns det väl bara ett ångtryck om och endast om det finns kokning (i en sluten behållare). Så vad menar man när man säger att ångtrycket måste överstiga omgivningens tryck för att kokning ska ske; det finns väl inget ångtryck om det inte kokar?
Så det korta här är egentligen att kokning helt enkelt inte kan ske i en sluten behållare så länge temperatur och tryck är i jämvikt inom kärlet eftersom förekomsten av en annan gas utgör en spärr som hindrar ångtrycket fårn att överstiga eller ens komma godtyckligt nära totaltrycket.
Detta är funktionen hos en tryckkokare eller en autoklav.
Kokning sker effektivt endast under icke-jämvikts förhållanden eller när partialtryck från andra gaser långt understiger ångtrycket vilket är varför fenomenet är så komplext att modellera.
Vad är kokning? Är det helt enkelt fasövergången från vätskefasen till ångfasen?
Nej, eftersom vi behöver skilja mellan fenomenet avdunstning och kokning. I kort så är kokning en fasövergång som sker på ett visst sätt och vid ett visst tillstånd.
På sätt och vis kan man förstå skillnaden bättre genom att helt enkelt kolla på vatten som värms upp en kastrull. Redan innan man sätter på värmen så sker materiaflöde från vattnet till atmosfären. Vi säger att det avdunstar, eller om man om man vill använda en anglicism kan man säga att det evaporerar . När temperaturen stiger så ökar avduntningshastigheten så den blir högre och högre och några tiotals grader under kokpunkte blir flödet så intensivt att vi ser dimma bildas ovanför vattnet men vattnet i sig är 'lugnt' och det är fortfarande avdunstning. Ju närmare vi kommer kokpunkten ju med intensiv blir avdunstningen men vid kokpunkten har vi ett helt nytt fenomen där våldsamma ångbubblor bildas (och ofta kollapsar) inuti vätskevolymen medan avdunstningen endast skedde utefter väteskeyta-gas-gränssnittet. Detta är kokning.
Fenomenet kokning är inte bara fasövergången i sig utan att det sker på detta distinkta sätt
I slutna kärl blir dock fenomenen svårskiljda från varandra eftersom det krävs ett så extremt kort kokningsförlopp för en vätska att inställa sig i jämvikt med en gasfas av samma volumetriska storleksordning som vätskevolymen på grund av densitetsförhållandena. Kokning i ett slutet kärl kan därför se ut som avdusntning vid visuell inspektion.
Teoretisk diskussion av begrepp:
Rent experimentellt är ångtrycket hos en vätska trycket hos gasfasen av samma vätska när den befinner sig i jämvikt med en gas. Mätning av ångtrycket kan göras genom att placera vätskan i vakuum och mäta trycket hos den resulterande gasfasen efter att vätskan antingen har kokat bort
Den klassiska kvicksilverbarometer-metoden (som beskriven i Paulings General Chemistry sida 42) är för potentiellt giftig för att implementeras idag men är fortfarande illustrativ:
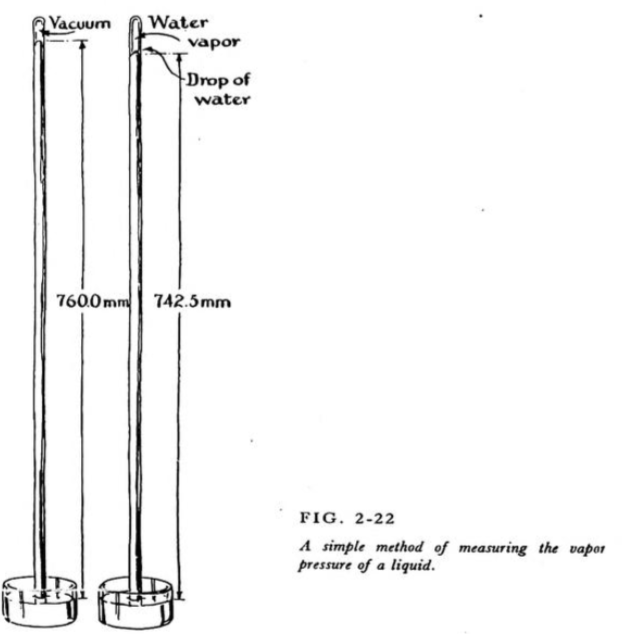
(Vätskedroppen kan injiceras med pipett från botten då den flyter upp till toppen)
Konceptuellt har ångtrycket två roller. (1) Det det beskriver det empiriska resulterande trycket vid jämvikt och (2) att ett högre ångtryck dynamiskt representerar ett större materiaflöde vid gas-vätska-gränssnittet. Vid jämvikt är materiaflödet i netto mellan faserna noll men kan modelleras dynamiskt som att två materiaflöden i olika riktningar är lika stora.
En vätska kommer i alla omständigheter att avdunsta eller koka tills dess att partialtrycket från dess gasfas når ångtrycket. På grund av Daltons lag om partialtryck kan man ignorera.
Jag vill understryka att skillnaden mellan kokning och avdunstning förstås från inspektion av skillnaden mellan kokning och avdustnings vid erfarenhet med experiment men om vi vill mekanisera verkligheten och presentera den som regelstyrd kan vi ge följande approximativa lagar:
- Om en vätskas ångtryck (definierat som en rent tabulerad intensiv egenskap) understiger partialtrycket från gasfasen av samma vätska så kommer det att ske en fasövergång där atomer i vätskan i netto lämnar vätskan. Detta kan ske genom antingen kokning eller avdunstning.
- Om det totala gastrycket, vätskans gasfas partialtryck plus partialtrycken från andra gaser) överstiger vätskans ångtryck så sker fasövergången genom avdunstning.
- Om det totala gastrycket understiger ångtrycket så sker kokning, vilket utmärks av helt nya vätska-gas-gränssnitt uppstår inuti vätskan i form av bubblor.
Jag inbjuder dig att göra tankeexperiment med vatten nära rumstemperatur
Tankeexperiment
E1: Vatten i ett slutet kärl i rent vakuum. Varför sker endast kokning?
E2: Vatten placeras i ett slutet kärl med en atmosfär med 1 atm vattenfri kvävgas med tryck 1 atm? Varför sker endast avdunstning.
E3: Vatten placeras i ett slutet kärl med atmosfär av vattenmättad kvävgas och initial jämvikt. Expandera kärlets volym isotermt så att gastrycket minskar. Sker kokning eller avdunstning?
E4: Vatten placeras i ett slutet kärl med atmosfär av mättad kvävgas med och initial jämvikt. Om temperaturen ökas långsamt vad händer
(den uppmärksamme läsaren inser att E3 introducerar en paradox i att E1 verkar omöjligt men när totalt gastryck och ångtryck inifinitessimalt nära varandra så blir jämviktarguments inte nödvändigtvis tillförlitliga)
Tack för ditt uttömande svar!
Medan jag funderar på ditt tankeexperiment har jag en allmän fråga. Låt säga att vi bereder en binär vätskeblandning av metanol och vatten med . Givet ett bestämt tryck (vi kanske låter vår blandning ligga i en behållare i kontakt med en tryckreservoir), finns det då en och endast en temperatur, där vätskan är i jämvikt med sin ånga, som är konsistent med ?
*Jämvikt i den termodynamiska bemärkelsen, alltså ett makroskopiskt stationärt tillstånd där det inte finns några makroskopiska flöden mellan eller inom faserna.
Jag har väldigt lite teoretisk eller praktisk erfarenhet med blandningar av vätskor så alla mina spekulationer är improvisativa.
Givet ett bestämt tryck P (vi kanske låter vår blandning ligga i en behållare i kontakt med en tryckreservoir), finns det då en och endast en temperatur, där vätskan är i jämvikt med sin ånga, som är konsistent med xMeOH=0.4?
Hur realiseras denna tryckreservoar? Om gasfasen inte inkluderar andra komponter än vätskans ånga så kan du inte kontrollera trycket, det blir ångtrycket (vid den temperaturen). Ta butan i en gascylinder vid 20 C. Trycket i den blir 1.74 atm inte för att vi har ställt in det på 1.74 atm utan eftersom det är vad det blir om vi ska ha en vätska-gas-blandning av butan vid 20 celsius.
Poängen med ångtryck är att det är en relation mellan tryck och temperatur som är oberoende av volymen.
Så vitt jag vet så implicerar Calusius-Claperions ekvation explicit att ångtrycket för en vätska (även för en blandning) är en monoton ökande funktion av temperaturen.
Något annat vore besynnerligt. Låt oss tänka oss att vi vid kvicksilver-mätningen av ångtryck applicerade en gaslåga mot röret så att droppen värms upp och efter att först ha sett kolumnen sjunka (indikerande ökande tryck) så skulle vid alltså vid någon senare punkt observera att trycket sjunker (vilket är vad som krävs för att vi ska få samma ångtryck vid olika temperaturer).
Frågan känns för mig alltså väldigt konstig men jag kanske missförstår den.
Jag tänker att vi kan använda exempelvis atmosfären som tryckreservoir. Vi bereder vår vätskeblandning i en icke-permeabel behållare omsluten av adiabatiska väggar där det i ena änden sitter en rörlig kolv som kan röra sig uppåt och nedåt. Vi kontrollerar temperaturen genom en värmeplatta:
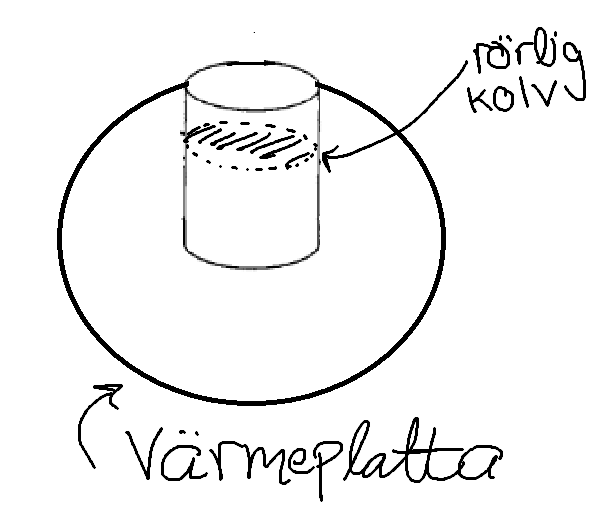
Om vi förutsätter att kolven kan röra sig så att cylinderns innehåll kan ställa in sig på vilken volym som helst, så kommer vi vid jämvikt få ett tryck inom cylindern som motsvarar atmosfärens tryck. Med en sådan uppställning borde vi väl kunna fixera jämviktstrycket?
Med en sådan uppställning borde vi väl kunna fixera jämviktstrycket?
Ja -- men endast om det finns en gaskomponent som inte kan lösa sig i vätskan och som kan utöva ett mottryck utan att drivas in i vätskan.
För en ren ånga kommer applicerade tryck som överstiger ångtrycket att helt kollapsa gasfasen.
Har du atmosfärstryck med 1 atm på kolven med vatten med temperatur 20 celsius så kommer kolven att hela vägen ner till vätskeytan och totalt eliminera gasfasen eftersom gasfasens mottryck maximalt är 0,02 atm(!) och därmed alltid mindre än 1 atm.
Enda sättet du kan ha en gasfas under dessa omständigheter är att höja temperaturen till kokpunkten (100 C) så att ångtrycket överstiger 1 atm. I praktiken är dock läget dynamiskt instabilt. Exakt vid kokpunkten är kolven i vila men precis över så kokar vattnet in i gasfasen så snabbt som energi kan dras från värmeplattan och gasvolymen expanderar eftersom den fylls upp av vattenånga
En klassisk ångmotor av Watt-typ utnyttjar explicit denna obalans för att extrahera energi om än baklänges genom att kylning av en vatten-vätska från 100 C till ~20 C imposivt minskar ångtrycket från 1 atm till 0,02 atm får ångkammaren att implodera och dra med sig kolven inåt.
Gif-bild på en enkel ångmotor bakom spoiler
Visa spoiler

https://commons.wikimedia.org/wiki/File:Newcomen_atmospheric_engine_animation.gif
Jag vet att du tycker att teori är häftigt men jag vill verkligen uppmuntra dig att så tidigt som möjligt adoptera perspektivet att fysik är nedströms från teknik och att studera teknologi är mycket bättre på att ge oss intution för hur fysikaliska principer fungerar.
En annan version för att åstadkomma en ett rörligt vatten-ånga-gränssnitt är att vända ett uppochnedvänt glas i en vakuumkammare.
Vid lufttryck 1 atm finns ingen ångfas ovanför vattnet. Även om trycket runt vattnet sänks till 0,1 atm uppstår ingen ångfas eftersom trycket fortfarande är större än ångtrycket. Gasfasen uppstår endast när omgivnande trycket sjunker under ångtrycket då gasfasen plötsligen uppstår och faller nedåt.
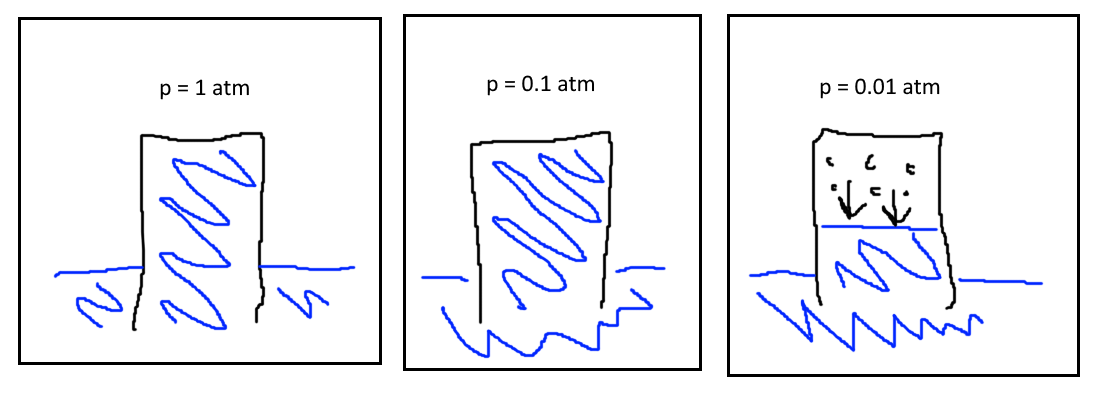
Okej, men jag tror att vi håller med varandra då.
Jag lyckades få tag på en kemiingenjör som hjälpte mig tolka VLE-diagram på formen (i och med min fråga):
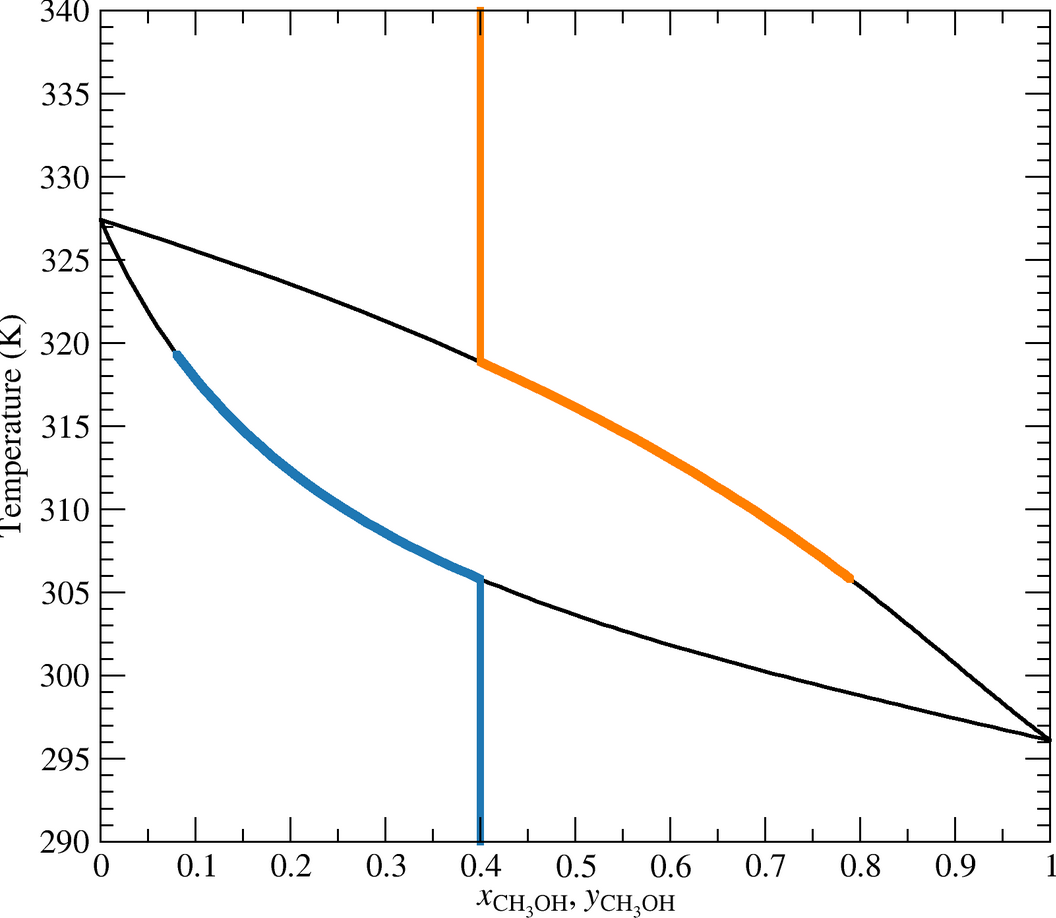
Detta är ett VLE-diagram för en binär blandning bestående av 40 mol% metanol och 60 mol% vatten, och visar vad som händer då man succesivt ökar temperaturen isobart vid något tryck under 1 atm.
Vid en låg temperatur befinner sig hela lösningen i vätskefas, och då existerar det ingen ångfas. Vid ca. 305 K har vi nått bubbelpunkten under de givna betingelserna, och i just detta fall är det den enda temperaturen som finns, där ångfas står i jämvikt med vätskefas OCH vi har . Om vi forsätter höja temperaturen kommer jämviktskompositionen i ång- och vätskefasen kontinuerligt förändras tills att vi når daggpunkten, och då är allt ånga.
Jag tror även att jag lyckats begripa vad skillnaden mellan ångtryck och mättnadstryck är nu, vilket var en av de saker som huvudsakligen förvirrade mig.
Mättnadstrycket för ett kemiskt species är trycket vid vilket vätskefasen och gasfasen står i jämvikt givet en viss temperatur. Detta tryck är alltså idealt endast temperaturberoende.
Ångtrycket för en blandning är trycket vid vilken ångfas är i jämvikt vid vätskefas givet en viss komposition och temperatur. Vi kan ha jämvikt mellan ångfas och vätskefas vid andra tryck också, men det är inkonsistent med vår komposition. T.ex. har vi ju Raoults lag för ideala (och binära) blandningar:
Tillägg: 24 feb 2026 15:17
Men detta verkar mycket märkligt. Vad gäller mättnadstrycket tror jag att det jag har skrivit stämmer, men jag kanske fortfarande är begreppsligt förvirrad vad gäller "ångtryck". Jag har sett vissa kalla det för "bubbelpunktstryck" och det verkar mycket mer rimligt. Personen jag skrev med kallade det konsekvent för "ångtryck".
Tillägg: 24 feb 2026 15:45
I den tyska Wikipediaartikeln står det faktiskt uttryckligen, angående ångtryck:
Der Dampfdruck ist der Druck, der sich einstellt, wenn sich in einem abgeschlossenen System ein Dampf mit der zugehörigen flüssigen Phase im thermodynamischen Gleichgewicht befindet



