Varför är C negativt laddad
Hej, hur vet jag att det är kolet som är negativt laddad? 4.10a

Testa att rita Lewisstrukturen och dela ut formella laddningar, så blir det nog tydligt.
Emmm. Vet inte riktigt hur man gör det med bara kol och kväve.
Du ritar det precis på samma sätt som med alla andra lewisstrukturer. Börja med att räkna ihop hur många valenselektroner som finns tillgängliga. Vilka olika bindningsordingar kan du välja bland? Vilken av dessa borde vara "den rätta"? (med avseende på minimerad formell laddning).
https://www.youtube.com/watch?v=fjGinmssUs0
Denna video kan hjälpa.
Jo, tänkte lite fel.
En fråga om d-uppgiften, är det viktigt att rita ut trippelbindningen mellan CN när jag ritar ut H3C--CN?
Hejsan266 skrev:Hej, hur vet jag att det är kolet som är negativt laddad? 4.10a
Det är en negativ jon så jag skulle tro att båda atomer har negativ laddning.
En fråga om d-uppgiften, är det viktigt att rita ut trippelbindningen mellan CN när jag ritar ut H3C--CN?
Ja, om du ska rita ut strukturformeln så ska du rita alla bindningar. (eller, det finns olika typer av strukturformler, så det är ju inget "måste" kanske, men det kan absolut inte skada.)
Det är en negativ jon så jag skulle tro att båda atomer har negativ laddning.
Den negativa laddningen är faktiskt lokaliserad på kolet.
naytte skrev:
Det är en negativ jon så jag skulle tro att båda atomer har negativ laddning.
Den negativa laddningen är faktiskt lokaliserad på kolet.
https://pubs.rsc.org/en/content/articlelanding/1977/dt/dt9770000220
Kvantkemiska beräkningar säger -0,6 e och -0,4 e.
Om man tittar på molekylära orbitaler blir det typ så här:
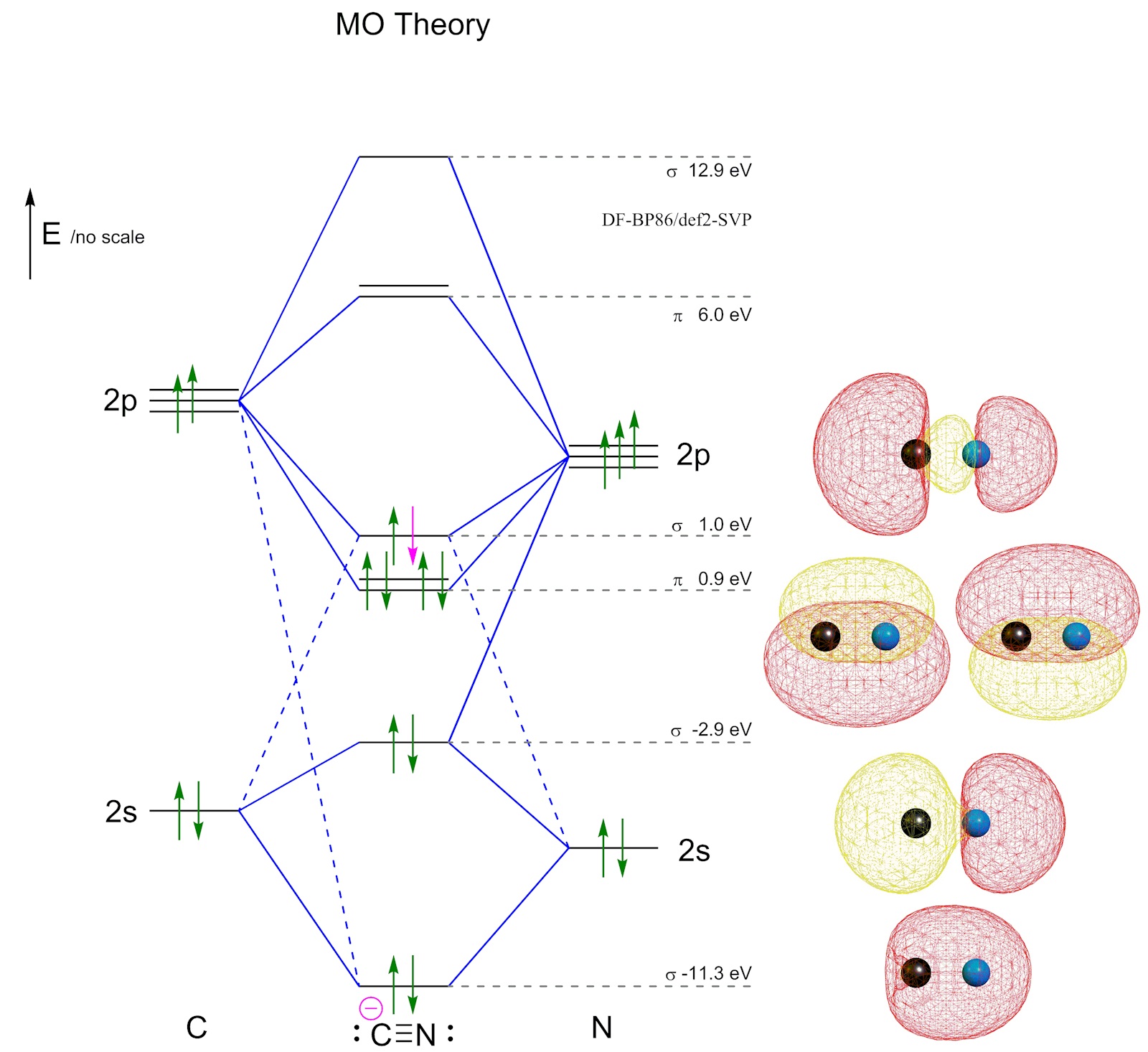 Den extra elektronen befinner sig i en sigma orbital som är en kombination av båda atomers 2p och 2s orbitaler.
Den extra elektronen befinner sig i en sigma orbital som är en kombination av båda atomers 2p och 2s orbitaler.
Den elektroniska strukturen är ganska lik den av N2. En av atomerna har en proton mindre. Det skulle ge C en laddning -e om inget annat skulle ändras. Men självklart flyttar en del av elektronmolnet med.
@Hejsan
När du betraktar cyanidjonen kemiskt, och mer specifikt som i frågan om nukleofilt reagens, behöver du utgå ifrån att kol har den negativa laddningen/extra elektronen. Anledningen till varför elektronen/laddningen behöver finnas på kolatomen för att reaktionen skall ske, kan förklaras med orbiltalteori, men det ligger på universitetsnivå.
Ofta används Lewisstrukturen för cyanidjonen för att illustrera hur elektronerna finns runt kol och kväve (vilket var vad Naytte uppmuntrade dig att undersöka). Även beräkningar av formell laddning används och ger samma resultat - att kolet har den formella laddningen -1.
Jag använde begreppet "formella laddning" för det är en ett förenklat sätt att beskriva laddningen, som undviker både orbitalteori, kvantmekanik och liknande teoretiska beskrivningar av hur elektronerna anses bete sig oftast under beräkningar i en idealiserad miljö. Det finns andra komplexa joner (=mer än en atom) som har en formell laddning, men inte en jämn fördelning av denna laddning inom jonen, och dessa kan också beskrivas så som Pieter Kupiers illustrationer visar, men i sambandet nukleofiler räcker det att fokusera på den formella laddningen.
Jo, men det är inte rätt att tro på https://en.wikipedia.org/wiki/Formal_charge och att hävda realism och att laddningen är ”faktiskt lokaliserad” på kolet.
Till exempel när man vill veta dipolmoment.
Lokalisering av elektroner är också en teknisk term med ett antal olika betydelser i molekyler och kristaller.
Pieter Kuiper skrev:Jo, men det är inte rätt att tro på https://en.wikipedia.org/wiki/Formal_charge och att hävda realism och att laddningen är ”faktiskt lokaliserad” på kolet.
Till exempel när man vill veta dipolmoment.Lokalisering av elektroner är också en teknisk term med ett antal olika betydelser i molekyler och kristaller.
Sammanhanget avgör hur rätt/fel eller användbara beskrivningarna är skulle jag säga.
Det går så klart att beräkna/beskriva mer precist var elektronerna har högst sannolikhet att befinna i ett givet och väl definierat system.
Men, i samband med att den nya bindningen från nukleofilen börjar bildas och orbiltalöverlappen inträffar, sker det inte med elektroner från kvävet utan de facto med elektroner från kolet - vi vet ju till vilken den enda produkten blir.
Så jag tycker det blir missvisande att påstå att man skulle behöva "tro" på den ena beskrivningen eller den andra för att kunna besvara frågeställningen. Det finns i ur min synvinkel inget motsatsförhållande mellan den förenklade produktorienterade "laddningen på kolet" beskrivningen, och en beräknad elektrondistribution för jonen. Den beräknade distributionen är beskaffad med ett antal antaganden och parametrar nödvändigt för definitionen av systemet, men dessa parametrar överensstämmer knappast väl med de mer kaotiska betingelserna som föreligger när frågans reaktion sker.
För att förtydliga vad jag menade bara för protokollet:
Jag pratade om lokalisering med avseende på lewisstrukturen. Det var uppenbarligen det frågan fiskade efter med tanke på att det handlar om en nukleofil substitution och det är så man ritar jonen i mekanismen. Det var inte ett påstående om verkligheten.




