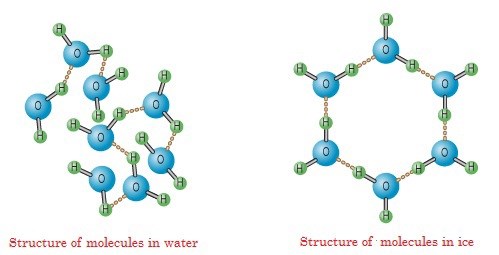
varför är vatten mer "dense" än is?
hörde att det va med vätebindingarna att göra. Att i fast form orienterar molekylerna så att syret möter den andras väte. Men fattar inte hur vatten kan vara mer tätt än fast form H20???
skulle hjälpa med en illustration :)
Enkelt sagt är det för att den ordnade hexagonala kristallstrukturen hos is tar upp en större volym än vad samma massa vatten gör. Mag1 ger bra svar i denna tråd med tillhörande bilder:
https://www.pluggakuten.se/trad/varfor-har-is-lagre-densitet-an-vatten/
Ebola skrev:Enkelt sagt är det för att den ordnade hexagonala kristallstrukturen hos is tar upp en större volym än vad samma massa vatten gör. Mag1 ger bra svar i denna tråd med tillhörande bilder:
https://www.pluggakuten.se/trad/varfor-har-is-lagre-densitet-an-vatten/
en sista fråga, gäller detta för alla vätebunda molekyler i fast form? det känns som det borde men är ej säker...
Nej, det är inget annat som är så extremt som vatten p g a symmetri. Alkoholer kan inte bilda ett lika regelbundet mönster. Varken alkoholer eller ammoniak kan inte bilda lika många vätebindningar.