Varför har aminer en större benägenhet att protolyseras än ammoniak?
Hej, i min kemibok står det att :
Aminer är ofta något starkare baser än ammoniak, eftersom de har en större benägenhet att protolyseras.
Jag undrar varför de har en större benägenhet att prololyseras än ammoniak?
Okej, men vad är det som är induktiv effekt hos aminer som inte är hos ammoniak? Är det att aminer har ett väte mindre än ammoniak?
Snarare att aminer har en elektronfrånstötande alkylgrupp, vilket ger ökad elektrotäthet kring kvävet som då får lättare att attrahera positiva vätejoner.
Tillexempel här har jag försökt rita deras protolys.
1. Ammoniak
2. Metylamin
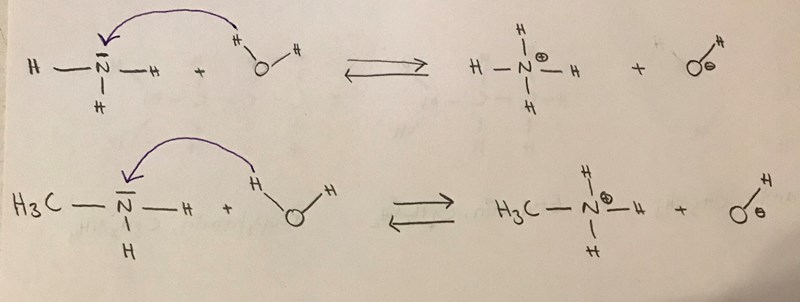
Vad menar du med elektronstötande alkylgrupp och elektrotäthet kring kvävet?
När man pratar om induktiv effekt så kan en funktionell grupp ge antingen en negativ effekt (d.v.s. dra till sig elektroner) eller positiv effekt (d.v.s. skjuta ifrån sig elektroner). Aminer är organiska föreningar innehållande alkylgrupper, vilka ger en positiv effekt. Du kan nästan se det som att kväveatomen blir "laddad" med elektroner. I ditt exempel så är metylgruppen bättre än en väteatomen på att ge iväg (samt ger iväg fler) elektroner till kvävet. Då blir kvävet så pass negativt laddat att den lätt kan dra till sig positiva joner såsom vätejoner, eller svagt positiva väteatomer som i ditt fall.
Jaa okej. Kan man då säga att kvävet blir delta negativt på grund av att den drar till sig elektronerna närmare sig och om man tittar på vattenmolekylen så är det syre som är delta negativt och väterna delta positiva? Att kvävet drar till sig delta positiva väteatomer?
Ja, precis.
Okej, tack så mycket för hjälpen! :)



